


Alcocer-Rodríguez Marisol1, Villalón-Rivera Alan1, Aguilar-Sánchez Cinthya1, Alejo-García Alma2, Cárdenas-Bernal Javier1
Trabajo presentado en el LIV Congreso Nacional Mexicano de Patología Clínica" y ganador del premio "Colegio de Médicos Patólogos Clínicos de Jalisco, A.C.
Introducción: La calidad y la confiabilidad de los resultados analíticos de serología infecciosa procesada son esenciales para la seguridad del paciente. La evaluación de la calidad y efectividad de los métodos analíticos se puede realizar mediante programas de ensayos de aptitud (PEA), que permiten comparar el desempeño propio con el de otros laboratorios.
Objetivo: Es establecer requisitos de calidad a través del estado del arte en serología infecciosa utilizando las encuestas de un PEA acreditado para la estimación de la especificación de desempeño analítico (EDA), expresándolo en 2 formatos diferentes: porcentaje y concentración.
Materiales y método: De los reportes de resultados emitidos por el PEA "EvECSI" (Evaluación Externa de la calidad en serología infecciosa) de las encuestas de 2024, se recabaron datos obtenidos para las pruebas HIV, HCV, HBsAg, Chagas y Sífilis, con los cuales se logró calcular las EDA en 2 formatos.
Resultados:
Se evaluó el desempeño durante el primer semestre de 2024 de VIH, utilizando el EDA obtenido contra el error sistemático y aleatorio, mostrando una aceptabilidad en los resultados.
Conclusiones: Al no contar con requisitos de calidad para serología en bibliografías, es indispensable definir un protocolo que permita establecer requisitos de calidad y evaluar el comportamiento del error aleatorio y del error sistemático contra las EDA obtenidos.
Introduction: The quality and reliability of processed infectious serology analytical results are essential for patient safety. The evaluation of the quality and effectiveness of analytical methods can be performed through proficiency testing programs (PTP), which allow for the comparison of one's performance with that of other laboratories.
Objective: To establish quality requirements through the state of the art in infectious serology using the surveys of an accredited PTP for the estimation of analytical performance specifications (APS), expressing it in two different formats: percentage and concentration.
Materials and method: From the 2024 surveys of the PTP “EvECSI,” data obtained for HIV, HCV, HBsAg, Chagas, and Syphilis tests were collected, which enabled the calculation of APS in two formats.
Results:
The performance of HIV during the first semester of 2024 was evaluated using the APS obtained against systematic and random errors, showing acceptability in the results.
Conclusions: Since there are no established quality requirements for serology in the literature, it is essential to define a protocol that allows for the establishment of quality requirements and the evaluation of random and systematic errors against the APS obtained.
En el ámbito de la medicina y la salud, especialmente en lo que respecta a la seguridad del paciente, la calidad y la confiabilidad son aspectos absolutamente críticos que no deben ser subestimados ni pasados por alto. La atención adecuada a estos elementos es fundamental para la correcta interpretación de los resultados y, por ende, para la toma de decisiones clínicas. Uno de los métodos más relevantes para evaluar el desempeño analítico de un laboratorio clínico es a través de los programas de ensayos de aptitud (PEA)1, esto se refiere a la evaluación de la calidad y efectividad de los métodos utilizados en laboratorios clínicos para asegurar resultados confiables, los cuales se miden a través de parámetros como la precisión, exactitud y la métrica sigma.
Es fundamental destacar que los requisitos de calidad que se establecen en los laboratorios clínicos deben estar estrictamente alineados con el uso previsto de las pruebas que se realizan. Esta alineación es esencial para asegurar que los resultados obtenidos sean adecuados y pertinentes para el propósito específico para el cual se llevó a cabo la prueba y que cumplan de este modo con los estándares de calidad que se consideran necesarios en la práctica clínica. Por lo tanto, resulta crucial que los laboratorios no solo definan, sino que también monitoreen de manera rigurosa sus requisitos de desempeño, de modo que se garantice la confiabilidad y la precisión de los análisis realizados.2
La especificación de desempeño analítico (EDA) puede ser expresada en forma de Error Total admisible (ETa), Error Sistemático máximo tolerable (ESa) o Sesgo máximo permitido y Error Aleatorio máximo tolerable (EAa)3. La elección de una especificación adecuada no es sencilla, existiendo múltiples criterios de decisión. Estos criterios se dividen en 5 niveles de acuerdo a la Conferencia Internacional de Consenso sobre Estrategias para Establecer Especificaciones Globales de la Calidad Analítica de 1999.
La mayoría de los métodos que actualmente se encuentran disponibles para el tamizaje serológico permiten la obtención de variables continuas, un número que corresponde a una señal detectada contra un punto de corte que determina si el mensurado se encuentra presente o ausente en la muestra, lo cual permite la aplicación de estadísticas que conllevan a la obtención de indicadores de desempeño para el conocimiento y seguimiento de éste; teniendo en cuenta que estas mediciones son semicuantitativas, el tener una especificación de desempeño analítico en serología infecciosa es fundamental para asegurar la precisión, exactitud, y confiabilidad de los resultados, cumplir con normativas y regulaciones, optimizar recursos y mantener la confianza en los servicios del laboratorio. Además, contribuye a la seguridad del paciente y al manejo adecuado de resultados críticos, y fomenta la mejora continua en el desempeño del laboratorio.5
Debido a la importancia de evaluar el desempeño de las pruebas de serología infecciosa y a la falta de fuentes que establezcan un requisito que se encuentre dentro de los primeros 4 niveles en los criterios de decisión para seleccionar una especificación de desempeño analítico (EDA), el presente trabajo se enfoca en la obtención de su propio EDA haciendo uso de la elección del nivel 5 de prestaciones basadas en el estado del arte, utilizando los datos del PEA “EvECSI” reportados como parte de su seguimiento de control de calidad externo del laboratorio Microtec.
Para el presente trabajo se tomaron resultados reactivos reportados y aprobados en el programa de ensayo de aptitud “EvECSI” de las pruebas serológicas HIV, HCV, HBsAg, Chagas y Sífilis; los datos fueron obtenidos del laboratorio de referencia Microtec, procesados en un equipo acreditado “Abbott Alinity I, No. de serie AI24361”, durante las encuestas realizadas del mes de febrero al mes de agosto de 2024 por parte del programa de calidad externa.
Posteriormente se conjuntaron el programa de estadística GMonitor realizado por GMigliarino Consultores, en el cual se realizó toda la estadística completa, siguiendo el paso a paso como se ejemplifica a continuación.
1. Obtención de los datos
Se recabó la información del valor informado, la media del grupo, el % de coeficiente de variación (%CV), la desviación estándar (SD) y el número de participantes de cada una de las encuestas reportas en el programa de ensayo de aptitud “EvECSI” durante el periodo descrito. Una vez conjuntados los datos estos fueron ingresados de manera manual al software GMonitor, para su posterior análisis estadístico.
TABLA 1: Resultados reactivos del marcador HCV, reportados en "EvECSI".
| Encuesta | Valor informado | Media grupo | %CV | SD | Participantes |
|---|---|---|---|---|---|
| feb-24 | 11.32 | 12.368 | 11.3 | 0.8658 | 23 |
| may-24 | 11.62 | 12.569 | 8.8 | 0.8798 | 18 |
| may-24 | 11.98 | 12.625 | 6.8 | 0.8838 | 18 |
| ago-24 | 11.54 | 12.259 | 7.6 | 0.8581 | 29 |
| ago-24 | 12.45 | 12.463 | 9.2 | 0.8724 | 29 |
2. Estimación de la media ponderada de la variable Desviación Estándar de grupo (SDg)
Para llevar a cabo la estimación, el software GMonitor inicialmente va a estimar la media ponderada de la variable Desviación Estándar de grupo (SDg) a partir de la siguiente ecuación:6
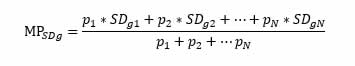
Donde:
TABLA 2: MPSDg de los resultados reactivos del marcador HCV reportados en “EvECSI”.
| Encuesta | SD | Participantes | SD* Participantes |
|---|---|---|---|
| feb-24 | 0.866 | 23 | 19.9134 |
| may-24 | 0.880 | 18 | 15.8364 |
| may-24 | 0.884 | 18 | 15.9084 |
| ago-24 | 0.858 | 29 | 24.8849 |
| ago-24 | 0.872 | 29 | 25.2996 |
| Suma | 117 | 101.8427 | |
| MPSDg | 0.8705 | ||
2.1 Estimación de una especificación de desempeño analítico
Finalmente, para estimar una Especificación de Desempeño Analítico para error total (EDA), el software GMonitor recurre a la siguiente ecuación:6
EDAcc = MPSDg * 3.0 Factor de cobertura: 3.0
TABLA 3: EDAcc de los resultados reactivos del marcador HCV reportados en “EvECSI”.
| HCV | |
|---|---|
| MPSDg | 0.8705 |
| Factor de cobertura | 3 |
| EDAcc | 2.61 |
3. Estimación de la media ponderada de la variable Coeficiente de Variación Relativo Porcentual de grupo
Para llevar a cabo la estimación, el software GMonitor inicialmente va a estimar la media ponderada de la variable coeficiente de variación relativo porcentual de grupo (%CV) a partir de la siguiente ecuación:6
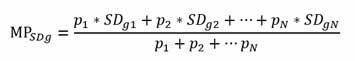
Donde:
TABLA 4: MP %CV de los resultados reactivos del marcador HCV reportados en “EvECSI”.
| Encuesta | %CV | Participantes | CV* Participantes |
|---|---|---|---|
| feb-24 | 11.3 | 23 | 259.9 |
| may-24 | 8.8 | 18 | 158.4 |
| may-24 | 6.8 | 18 | 122.4 |
| ago-24 | 7.6 | 29 | 220.4 |
| ago-24 | 9.2 | 29 | 266.8 |
| Suma | 117 | 1027.9 | |
| MP%CV | 8.7855 | ||
3.1 Estimación de una especificación de desempeño analítico
Finalmente, para estimar una Especificación de Desempeño Analítico para error total (EDA) el software GMonitor recurre a la siguiente ecuación:6
EDAcc = MP%CV * 3.0 Factor de cobertura: 3.0
TABLA 5: %EDA de los resultados reactivos del marcador HCV, reportados en “EvECSI”.
| HCV | |
|---|---|
| MP%CV | 0.7855 |
| Factor de cobertura | 3 |
| %EDA | 26.4 |
Estas mismas operaciones del paso a paso las realizó el software GMonitor de manera automática para los datos ingresados de las demás pruebas serológicas que se utilizaron para el presente trabajo (HCV, HBsAg, Chagas y Sífilis) obteniendo el EDAcc, así como el %EDA para los valores reactivos que fueron reportados al programa de ensayo de aptitud utilizado.
Después de realizar la estadística por medio del software GMonitor, se obtuvieron los resultados que se muestran en la Tabla 6, sobre la especificación de desempeño en concentración (EDAcc) y la especificación de desempeño en porcentaje (%EDA) para los 5 marcadores serológicos que fueron objeto de estudio para este trabajo, también se pudo obtener el error sistemático máximo tolerable en porcentaje (%ESa) así como el error aleatorio máximo tolerable en porcentaje (%EAa).
TABLA 6: Resultados de EDAcc y %EDA para los marcadores de serología infecciosa reportados en “EvECSI”.
| Marcador | Reactivos | |||
| EDAcc | %EDA | %ESa | %EAa | |
| HIV | 13.89 | 25.7 | 12.9 | 6.4 |
| HCV | 2.61 | 26.4 | 13.2 | 6.6 |
| HBsAg | 9.43 | 23.8 | 11.9 | 6.0 |
| Chagas | 2.27 | 18.4 | 9.2 | 4.6 |
| Sífilis | 4.09 | 17.7 | 8.9 | 4.4 |
Una vez obtenidos los datos, se evaluó el desempeño analítico mensual durante el primer semestre del año, se comparó el %EAa contra el %CV obtenido del CCI en cada marcador de manera mensual durante el lapso estipulado. En la Tabla 7 se muestra el conjunto de los datos obtenidos para el marcador de HIV, donde se aprecia que todos los %CV son menores que el %EAa, dando como aprobado este desempeño. En la Figura 1 se ejemplifica la evaluación de manera visual de los datos representados en la Tabla 7.
TABLA 7: Evaluación de desempeño analítico de los %CV mensuales de HIV contra el %EAa.
| Marcador | Nivel CCI | %EAa | %CV | |||||
| Enero | Febrero | Marzo | Abril | Mayo | Junio | |||
| HIV | Positivo + | 6.4 | 4.4 | 4.1 | 6.0 | 6.2 | 3.9 | 3.2 |
| HIV | Positivo ++ | 6.4 | 5.0 | 6.2 | 5.2 | 5.3 | 3.7 | 3.5 |
| HIV | Positivo +++ | 6.4 | 3.8 | 4.1 | 4.9 | 3.9 | 5.2 | 5.5 |

FIGURA 1: Evaluación del desempeño analítico de los %CV mensuales de HIV contra el %EAa.
De la misma forma se comparó el %ESa contra los sesgos obtenidos de manera mensual durante el mismo lapso de tiempo del programa interlaboratorios del cual el laboratorio Microtec forma parte, utilizando los controles de calidad externos ACCURUN 3. En la Tabla 8 se muestra el conjunto de los datos obtenidos para el marcador de HIV, donde se aprecia que todos los %Sesgos son menores que el %ESa, dando como aprobado este desempeño.
En la Figura 2 se ejemplifica la evaluación de manera visual de los datos representados en la Tabla 8.
TABLA 8: Evaluación de desempeño analítico de los %CV mensuales de HIV contra el %EAa.
| Marcador | Nivel CCI | %ESa | Sesgo | |||||
| Enero | Febrero | Marzo | Abril | Mayo | Junio | |||
| HIV | Positivo | 12.85 | -7.08 | -2.67 | -0.89 | 2.34 | 4.21 | 6.94 |

FIGURA 2: Evaluación de desempeño analítico de los %Sesgos mensuales de HIV contra el %ESa.
La especificación de desempeño analítico (EDA) debe basarse en criterios bien definidos que reflejen tanto las necesidades clínicas como las regulaciones vigentes. La implementación de un EDA sólido, en particular para pruebas de serología infecciosa, es fundamental no solo para la precisión y exactitud de los resultados, sino también para optimizar recursos y fomentar la mejora continua en el laboratorio, el cual puede establecer sus propios requisitos de calidad, a partir del estado del arte.
Conocer el comportamiento del CV% (error aleatorio) y el sesgo (error sistemático) contra las especificaciones de desempeño analítico permiten dar un seguimiento oportuno a los analitos; así como la detección de tendencias y aplicar acciones preventivas en el sistema analítico completo.
El desempeño analítico de los marcadores en serología infecciosa que fueron sometidos a evaluación en este trabajo, demuestran una aceptabilidad en los resultados evaluados, determinando que el mejor formato de expresión para evaluar un EDA para resultados reactivos es el porcentaje y para resultados no reactivos puede usarse un EDA en formato de expresión en concentración; sin que esto sea una limitante para que el laboratorio pueda determinar qué formato de los dos disponibles, es el más adecuado para evaluar el desempeños de sus pruebas en serología infecciosa.

Alcocer-Rodríguez Marisol
Villalón-Rivera Alan
Aguilar-Sánchez Cinthya
Cárdenas-Bernal Javier
Laboratorio de Inmunología hormonas, Grupo MICRO-TEC, México.
Alejo-García Alma
Departamento de Asesoramiento Externo, Grupo LICON, México.
CONTACTO
Dra. Sandra Quintana Ponce
Facultad de Ciencias Naturales, Universidad Autónoma de Guerrero, México. Av. Universidad S/N Ex Rancho el Shalako. Las Petaquillas, Guerrero.
E-mail: squintanap@uagrovirtual.mx
RECEPCIÓN: Enero de 2024
ACEPTADO: Mayo de 2024
Introducción del autor